方向一:多对比度光学成像系统
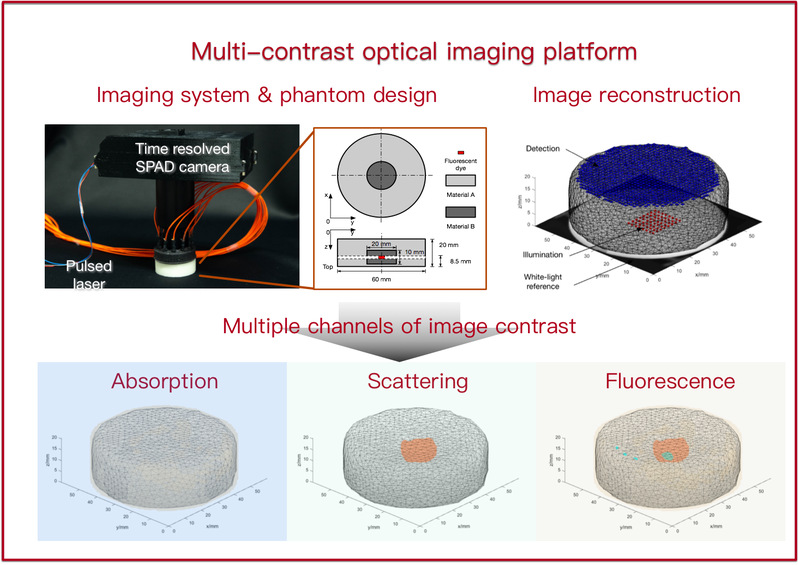
我们的目标是开发一种能够可视化生物组织中多个对比度参数的新型光学成像平台。 该平台集成了波长可调脉冲激光器和飞行时间相机等最先进的硬件组件,以及新颖的重建算法和精确的校准方法。 这种平台的主要应用包括小动物成像和图像引导手术。
参考文献:
1. W. Ren, J. Jiang, A. D. Costanzo Mata, A. Kalyanov, J. Ripoll, S. Lindner, E. Charbon, C. Zhang, M. Rudin, and M. Wolf, Multimodal imaging combining time-domain near-infrared optical tomography and continuous-wave fluorescence molecular tomography, Opt Express 28, 9860-9874 (2020).
2. W. Ren, H. Isler, M. Wolf, J. Ripoll, and M. Rudin, Smart Toolkit for Fluorescence Tomography: Simulation, Reconstruction, and Validation, IEEE Trans Biomed Eng 67, 16-26 (2020).
3. W. Ren, L. Li, J. Zhang, M. Vaas, J. Klohs, J. Ripoll, M. Wolf, R. Ni, and M. Rudin, Non-invasive visualization of amyloid-beta deposits in Alzheimer amyloidosis mice using magnetic resonance imaging and fluorescence molecular tomography, Biomed Opt Express 13, 3809-3822 (2022).
方向二:光学-MRI混合系统
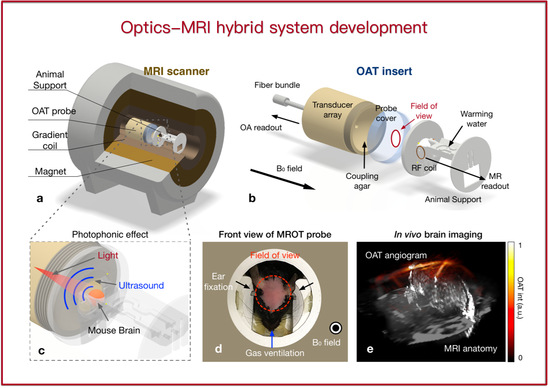
多模态成像已成为生物医学研究和临床使用的一种强大方法。与单一模态相比,可以获得更全面的生理信息。我们将光学和 MRI 相结合有多方面的优点。 首先,光学成像,特别是荧光成像,具有高灵敏度和特异性,与MRI高度互补。 其次,MRI 可以提供准确的解剖学参考,有助于定位荧光信号。 第三,MRI和光学成像都可以避免电离辐射。 我们的团队此前开发了世界上第一台荧光断层扫描-MRI系统和光声断层扫描-MRI系统。
参考文献:
1. W. Ren, X. L. Dean-Ben, M. A. Augath, and D. Razansky, Development of concurrent magnetic resonance imaging and volumetric optoacoustic tomography: A phantom feasibility study, J Biophotonics 14, e202000293 (2021).
2. Y. Hu, B. Lafci, A. Luzgin, H. Wang, J. Klohs, X. L. Dean-Ben, R. Ni, D. Razansky, and W. Ren, Deep learning facilitates fully automated brain image registration of optoacoustic tomography and magnetic resonance imaging, Biomed Opt Express 13, 4817-4833 (2022).
3. W. Ren, B. Ji, Y. Guan, L. Cao, and R. Ni, Recent Technical Advances in Accelerating the Clinical Translation of Small Animal Brain Imaging: Hybrid Imaging, Deep Learning, and Transcriptomics, Front Med (Lausanne) 9, 771982 (2022).
方向三:AI赋能的图像重建
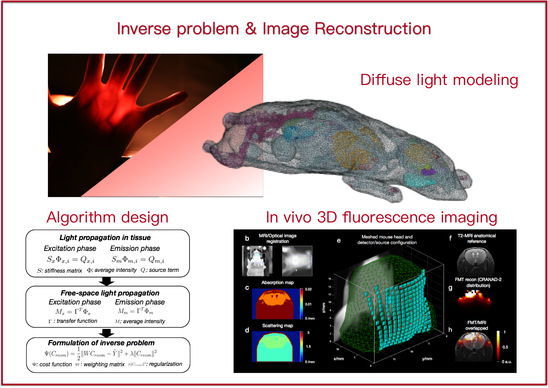
3D 重建的概念通常用于光学显微镜,例如共聚焦显微镜和双光子显微镜。 然而,由于组织中严重的光散射,可视化深入组织(> 1 毫米)的物体变得具有挑战性。 众所周知,散射介质中的这种宏观重建是高度不适定的逆问题。 我们正在寻求基于先进计算技术和新颖机器学习方法的快速、稳健、3D、高分辨率图像重建算法。
参考文献:
1. Y. Liu, W. Ren, and H. Ammari, Robust reconstruction of fluorescence molecular tomography with an optimized illumination pattern, Inverse Problems & Imaging 14, 535-568 (2020).
2. W. Ren, H. Isler, M. Wolf, J. Ripoll, and M. Rudin, Smart Toolkit for Fluorescence Tomography: Simulation, Reconstruction, and Validation, IEEE Trans Biomed Eng 67, 16-26 (2020).




 沪公网安备 31011502006855号
沪公网安备 31011502006855号


